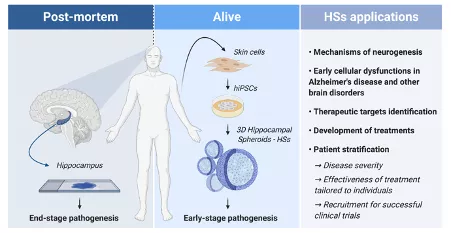
Vid Alzheimers sjukdom påverkas hippocampus, som är en struktur i hjärnan som reglerar motivation, känslor, lärande och minne, allvarligt. Kunskap om vilka cellulära förändringar som sker i ett mycket tidigt stadium vid Alzheimers sjukdom skulle möjliggöra utveckling av behandlingar som kan bromsa sjukdomen. Eftersom forskare inte har tillgång till vävnad från hippocampus, har det hittills inte varit möjligt att studera vad som händer när cellerna slutar fungera och nervcellerna skadas.
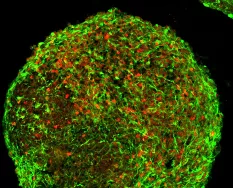
Forskare i Lund har nu lyckats utveckla så kallade hippocampala sfäroider (HS). Det är hippocampala vävnadsliknande strukturer i 3-D som utvecklats från inducerade pluripotenta stamceller (iPSC).
I de flesta ryggradsdjur, inklusive människor, utvecklas nya nervceller under hela livet genom en process som kallas neurogenes och dessa celler tros bidra till minnesbildning. Den nya metoden kommer att möjliggöra en större produktion av hippocampala nervceller som kan användas för att studera neurogenes hos människan. Framför allt ger modellen forskarna möjlighet att undersöka hur mänskliga celler från hippocampus kan drabbas i ett mycket tidigt skede vid Alzheimers sjukdom och andra sjukdomar där hippocampus är skadad.
- Genom att använda inducerade pluripotenta stamceller från patienter kan vi skapa unga hjärnceller och undersöka de tidiga sjukliga förändringar som sker och få värdefull insikt i utvecklingen av dessa hjärnsjukdomar, förklarar Laurent Roybon, forskargruppsledare för Stem Cell Laboratory for CNS Disease Modeling vid Lunds universitet och en av forskarna bakom studien.
Förståelse för patientspecifik sjukdomsbild
Forskarna använde också hippocampala sfäroider för att undersöka vad som inte fungerar i cellerna vid Alzheimers sjukdom och mer exakt hur detta skilde sig åt mellan olika individer. De genererade hippocampala sfäroider från patienter med olika former av Alzheimers och jämförde dem. De genererade HS från patienter med extrem symtomatologi dvs en typisk Alzheimers patient som bär en mutation i amyloidprekursorproteingenen och en atypisk individ som bär en sällsynt mutation i presenilin 1-genen - och undersökte den cellulära patologin.
- Intressant nog fann vi att trots att de visade några viktiga gemensamma särdrag skilde sig de hippocampala sfäroiderna från de två mutanterna sig åt i många andra egenskaper. Skillnaderna återspeglade svårighetsgraden av deras symtom i viss mån, förklarar Yuriy Pomeshchik, huvudförfattare till den nya studien.
Hippocampala sfäroider kan tjäna flera syften
Det arbete som utvecklats i Laurent Roybons laboratorium öppnar upp nya möjligheter, eftersom det tjänar flera syften:
- Hippocampala sfäroider kan användas för att förstå hur celler i hippocampus utvecklas och mognar över tiden. De kan också användas för att undersöka om neurogenesen påverkas i hippocampala sfäroider som utvecklas från patienter med hippocampal skada jämfört med friska individer. Analysen av de hippocampala sfäroiderna kan avslöja vilka cellulära fel som uppstår tidigt i sjukdomen och om de är identiska eller skiljer sig åt mellan patienter. Hippocampala sfäroider kan utnyttjas för att utveckla skräddarsydda behandlingar för undergrupper av patienter samt för att förstå varför vissa behandlingar skulle kunna vara till nytta för dem eller ej. I slutändan kan hippocampala sfäroider möjliggöra studier av hur effektiv en behandling är innan behandlingen påbörjas, utöver att den används som ett sätt att placera individer i undergrupper för klinisk prövning, och rekrytera de patienter som kan svara väl på behandlingen. Vi tror att hippocampala sfäroider kommer att vara ett viktigt verktyg för att utveckla nya behandlingar och ge patienter den bästa möjliga sjukvården, säger Laurent Roybon.
- Vi använde hippocampala sfäroider för att undersöka effekten av en gen som heter NeuroD1, som vi har studerat i flera år. Med hjälp av virala vektorer kunde vi öka uttrycket av genen av NeuroD1 och det var tillräckligt för att öka nivån av synaptiska gener, som är låga vid Alzheimers sjukdom. Att förbättra synaptisk överföring kommer att vara nyckeln till att lösa försämrad kognition vid Alzheimers sjukdom, säger Yuriy Pomeshchik.
- Vi kommer att fortsätt sikta mot att generera sfäroider från patienter som diagnostiserats med neurodegenerativa sjukdomar och använda dem för att få ökad kunskap om tidig cellulär dysfunktion men även för att fastställa sjukdomsspecifika behandlingsmål. Vi kommer också att fortsätta att arbeta för implementering av NeuroD1-genterapi som en behandling för patienter med neurodegenerativa sjukdomar, avslutar Laurent Roybon.
Genom att använda en liknande metod genererade forskarna också sfäroider i mellanhjärnan som innehåller dopaminproducerande nervceller för att identifiera tidiga metaboliska dysfunktioner i celler vid Parkinsons sjukdom (Chumarina et al., Acta Neuropathologica Communications, 2019).